| “改写教科书!Science Immunology封面级研究揭示:胎肝才是ILC真正的‘摇篮’” |
| ( 2025-08-03 ) |
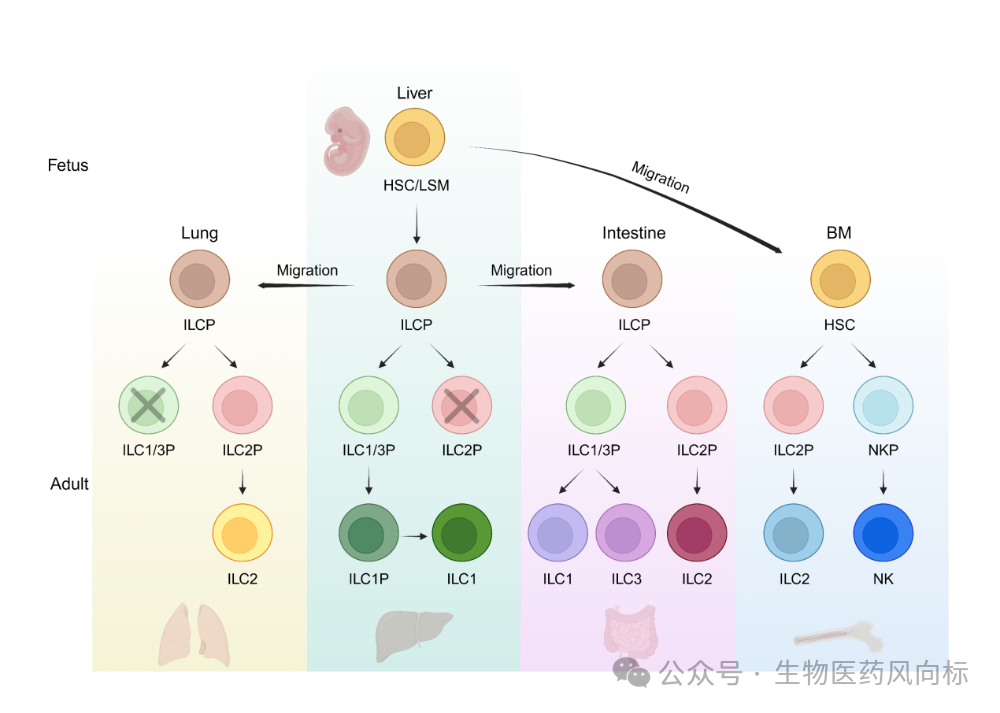
2025年7月11日,中国科学技术大学生命科学与医学部基础医学院、免疫应答与免疫治疗全国重点实验室田志刚教授、彭慧教授课题组,与法国艾克斯-马赛大学Eric Vivier教授团队合作,在《Science Immunology》在线发表了题为“Innate lymphoid cells originate from fetal liver–derived tissue-resident progenitors”的研究长文。该研究利用多组学谱系示踪、单细胞测序、体外胚胎期器官培养及遗传学模型,系统阐明了固有淋巴细胞(innate lymphoid cells, ILC)的胚胎起源与发育路径,首次提出并验证了“胎肝起源-组织驻留-骨髓非依赖”的新范式,颠覆了传统“骨髓中心论”对ILC发育的理解。以下从背景、研究设计、主要发现、意义与展望四个维度进行深度解读。 一、研究背景:从“骨髓中心论”到“多器官起源说” ILC是近年才被明确定义的一类组织驻留型固有免疫细胞,按表型与功能可分为ILC1、ILC2和ILC3三大亚群,在抗感染、抗肿瘤、组织修复及免疫调节中扮演关键角色。传统观点认为,出生后的ILC主要由骨髓共同淋巴样祖细胞(CLP)分化而来;然而,越来越多的证据提示外周组织存在骨髓非依赖的ILC补给自己制。田志刚团队2021年和2022年先后发现肝脏驻留NK细胞(即ILC1)来源于肝内原位造血前体,首次动摇了“骨髓唯一论”。但这些发现多聚焦于单一亚群、单一器官,尚缺乏对“所有ILC亚群是否共享一条胚胎期外骨髓起源路径”的系统回答。 二、研究设计:三大技术路线交叉验证 1. Fgd5-CreERT2命运示踪系统:Fgd5是造血干细胞(HSC)特异性标志。通过他莫昔芬诱导的Cre-loxP重组,研究者可在不同发育阶段永久标记Fgd5+ HSC及其子代,从而精确区分“胎肝造血波”与“骨髓造血波”对成年ILC库的贡献。 2. 单细胞转录组+TCR克隆追踪:对胎肝、胎肺、胎肠、成年骨髓及外周组织的Lin−CD127+ ILC前体(ILCP)进行单细胞RNA测序,并结合TCR重排信息排除混杂T细胞。 3. 体外胚胎器官培养与遗传缺陷模型:分离E12.5–E15.5胎肝与胎肺、胎肠,在3D基质胶中培养,追踪ILCP迁移与分化;同时利用Rag2−/−Il2rg−/−小鼠验证胎肝ILCP的重建能力。 三、主要发现:一条清晰的“胎肝-外周器官驻留”发育轴 1. 胎肝启动最早的ILC定向造血 命运示踪显示,E10.5–E12.5胎肝即出现PD-1+IL-7Rα+Id2+的ILC限制性祖细胞(ILCP),其分子特征与骨髓ILCP显著不同,表现为更高表达转录因子Tcf7、Zeb2及趋化受体Cxcr6,提示更强的组织迁移潜能。 2. ILCP“播种”外周器官并受微环境“教育” 胎肝来源的ILCP依次定植于胎肺和胎肠;局部微环境决定其分化命运: • 胎肠微环境诱导ILCP向ILC1/3双潜能祖细胞(ILC1/3P)分化,进而生成ILC1与ILC3; • 胎肺高表达IL-33与TSLP,驱动ILCP向ILC2祖细胞(ILC2P)倾斜。 这些外周ILCP及其下游祖细胞在出生后仍长期驻留,并在局部自我更新,贡献成年组织ILC库的65%–85%。 3. 骨髓ILC2发育路径独立且晚发 相比之下,骨髓来源的ILC2P/ILC2在出生后第2–3周才大量出现,其生成依赖于骨髓CLP及IL-7R信号,主要补充血液与脾脏而非实质器官。 4. 胎肝ILCP可重建全身ILC网络 将E13.5胎肝PD-1+ILCP移植至Rag2−/−Il2rg−/−新生鼠,可在肝脏、肺、肠道重建全部ILC亚群,且重建效率显著高于等量骨髓ILCP,提示胎肝路径在系统发育中的主导地位。
四、意义与展望:改写教科书的新框架 1. 理论层面:研究首次从时间与空间维度绘制了ILC发育的“双轨图”——一条胚胎期胎肝驱动的“外骨髓路径”,一条出生后骨髓主导的“经典路径”,为理解ILC个体发育与系统进化提供了全新框架。 2. 临床层面: •围产期干预:明确胎肝ILCP具有高度可塑性,为通过母体免疫调节或宫内干细胞移植防治新生儿感染、炎症性疾病提供新靶点; •肿瘤免疫治疗:组织驻留ILC与免疫检查点抑制剂、CAR-T疗法的协同效应日益受到关注,胎肝来源ILCP或可成为“现货型”细胞治疗新来源; •再生医学:利用胎肝ILCP体外扩增并定向诱导为特定亚群,有望用于修复炎症性肠病、哮喘等ILC失衡相关疾病。 3. 技术层面:Fgd5-CreERT2命运示踪与单细胞多组学整合策略,可作为研究其他组织驻留免疫细胞(如组织驻留记忆T细胞、组织巨噬细胞)发育起源的通用范式。 综上,该研究不仅回答了ILC“从哪里来”这一发育生物学核心问题,更为“如何用好ILC”奠定了理论基础与工程路线图,标志着我国科学家在固有免疫领域再次取得国际领跑成果。 -------上述内容转自“生物医药风向标”公众号 |